Как сходить с метипреда
Обновлено: 07.09.2024
В последнее время тактика лечения ревматоидного артрита значительно изменилась. Новое в лечении ревматоидного артрита – это отказ от выжидательной позиции и раннее назначение агрессивного курса терапии. Это привело к тому, что специалистами была признана обратимость патологического процесса на ранних стадиях заболевания при назначении активной терапии сразу после установления диагноза.
Ревматоидный артрит в цифрах
По современным представлениям ревматоидный артрит (РА) – это сложное многофакторное, хроническое, неуклонно прогрессирующее, системное аутоиммунное заболевание, в основе которого лежит длительный воспалительный процесс в организме с язвенно-деструктивным поражением и разрушением суставов.
Причины ревматоидного поражения связывают в основном с генетической предрасположенностью, вирусными инфекциями и многочисленными внешними пусковыми факторами. Код серопозитивного РА по МКБ - 10 M05.0, серонегативного - 10 M06.0.
Поражение РА населения составляет около 1% всего населения земного шара. Болеют лица любого возраста, от младенцев до пожилых людей, чаще женщины. По статистике ревматоидный артрит был установлен на 1-м году заболевания у 57,9% пациентов, остальные лечились по поводу недифференцированного (неустановленного вида) артрита (НДА), а это значит, не получали необходимой терапии. Еще через год у 33% больных этой группы был выявлен РА, то есть, их лечение замедлилось еще почти на год.
Новейшие принципы лечения РА
В последние десятилетия сформировались основные принципы терапии ревматоидных поражений, их придерживаются специалисты всего мира.
Принцип первый – ранее выявление
Лечить ревматоидные процессы непросто, результат во многом зависит от результатов обследования, установленного диагноза и предполагаемого прогноза болезни. Выявить ревматоидную патологию на ранней стадии сложно, так как похожие симптомы наблюдаются и при других заболеваниях. Поэтому очень большое значение придается выявлению РА и установлению развернутого диагноза, позволяющего сделать прогноз течения болезни у данного больного и назначить ему адекватные лечебные мероприятия.

Диагностика ревматроидного артрита
Диагноз ревматоидного артрита ставится на основании:
- Характерных симптомов болезни.
- Данных лабораторных исследований, подтверждающих наличие РА:
- низкий гемоглобин или снижение числа эритроцитов - анемия;
- ускоренная СОЭ, высокие показатели СРБ – признак воспаления;
- наличие/отсутствие ревматоидного фактора (РФ положительный или отрицательный);
- наличие/отсутствие антител к цитруллину (АЦЦП);
- наличие в крови цитокинов, поддерживающих воспаление (ФНО альфа, ИЛ-1 и др.).
- Данных инструментальных исследований, подтверждающих диагноз:
- рентгенография - выявляется рентгенологическая стадия суставных поражений;
- МРТ – самый точный метод, позволяющий выявить нарушения, еще незаметные на рентгене;
- УЗИ – выявляются изменения суставных и околосуставных тканей.
В диагнозе обязательно отражается активность патологического процесса, она очень важна для прогноза заболевания. Индекс активности ревматоидного артрита – DAS-28 рассчитывается позволяет оценить состояние пораженных суставов и общее состояние здоровья.
ФК (функциональный класс) ревматоидного процесса позволяет оценить сохранность трудовых навыков. По степени их нарушения выделяют 4 ФК.
Диагноз должен включать в себя клиническую и рентгенологическую стадии заболевания, активность патологического процесса, наличие/отсутствие РФ и системных поражений. Это позволит подобрать больному наиболее подходящую схему лечения.
Принцип второй – раннее назначение медикаментозной терапии
Схемы лечения ревматоидного артрита нового поколения учитывают клинически подтвержденный факт, что при раннем назначении активных лечебных мероприятий патологический процесс можно остановить и даже повернуть вспять. Поэтому главной целью является раннее выявление заболевания с назначением адекватного лечения, а непосредственными задачами:
- устранение болевого синдрома;
- подавление прогрессирования заболевания болезни;
- достижение состояния стойкой ремиссии;
- предупреждение двигательных нарушений;
- повышение качества жизни больного.
Современная тактика ведения ревматоидных поражений – это агрессивная тактика, когда больному назначается комплексное лечение с максимальными дозировками основных (базисных) противовоспалительных препаратов (БПВП). При этом противовоспалительные средства подбираются по результатам обследования. Раз в квартал проводится текущее обследование с целью проверки результативности проводимой базисной терапии. В состав медикаментозной терапии обязательно вводятся биологические препараты.
Раннее назначение агрессивной медикаментозной терапии
Принцип третий – сокращение симптоматической терапии
Новое в лечении ревматоидного артрита – это еще и подход к симптоматической терапии. Сейчас отказались от стандартных схем применения обезболивающих и общих противовоспалительных средств. Их назначают строго индивидуально при наличии воспалительной боли и обязательно сочетают с приемом базисных медицинских препаратов.
Допускается даже нерегулярный прием лекарств из группы нестероидных противовоспалительных препаратов (НПВП) – их принимают по мере необходимости максимально короткими курами или одноразово, используя только один препарат этой группы. Это связано с побочными эффектами НПВП – они вызывают эрозивно-язвенные поражения желудочно-кишечного тракта (ЖКТ). Еще одна опасность применения этой группы препаратов в том, что на ранних стадиях заболевания они быстро снимают все симптомы заболевания и создают иллюзию полного выздоровления. Это часто приводит к отказу больного от дальнейших лечебных мероприятий и прогрессированию ревматоидного процесса.
Еще одна группа препаратов для лечения ревматоидных поражений – глюкокортикостероиды (ГКС). Они оказывают, как симптоматическое, так (частично) и патогенетическое действие, подавляя процесс разрастания соединительной ткани в суставах, деструкцию хрящевой и костной ткани. На первых начальных стадиях ревматоидного процесса их назначают только при наличии выраженного болевого синдрома воспалительного характера – ГКС отлично снимают воспаление и боль, после чего их отменяют.
Но есть категории больных, в основном это лица преклонного возраста, которым не подходят препараты базисной терапии. В таких случаях эту роль берут на себя ГКС, назначаемые продолжительными курсами в низких дозировках. Иногда их вводят в суставы. Назначение их требует регулярного обследования больного из-за возможных побочек: остеопороза, язвенных процессов в ЖКТ и т.д.
В последние годы препараты этой группы все чаще назначают короткими курсами в высоких дозировках (пульс-терапия). Показаниями для таких процедур лечения являются тяжелые системные поражения (сердца, печени, почек).
Принцип четвертый – двигательная активность
Она необходима для профилактики контрактур и анкилозов (снижение объема движений в суставе или его полная неподвижность), а также мышечных атрофий необходима даже в период обострений – назначается щадящий комплекс лечебной физкультур – ЛФК. По мере улучшения состояния больного нагрузки увеличиваются.
Одновременно назначаются курсы лечебного массажа и физиотерапевтических процедур, усиливающих эффект ЛФК. Для сохранения нормального положения конечности назначают ношение ортезов, но только по нескольку часов в день – постоянное ношение ортезов считается неприемлемым. Двигательная активность значительно улучшает качество жизни больных с ревматоидными поражениями.
Препараты для медикаментозного лечения
Все препараты от ревматоидного артрита делятся на симптоматические и базисные. Симптоматические – это НПВП и ГКС, а базисные – синтетические и биологические.
Лекарственные средства этой группы угнетают образование фермента циклооксигеназы (ЦОГ). ЦОГ делится на два вида: ЦОГ-2, участвующую в синтезе простагландинов, поддерживающих воспаление и боль, и ЦОГ-1, поддерживающую синтез простагландинов, стимулирующих секрецию слизи в органах пищеварения и защищающих стенки органов от различных воздействий.
Первые препараты группы НПВП - Диклофенак, Кетанов, Ибупрофен и др. эффективно подавляли оба вида ЦОГ, поэтому давали много побочных эффектов со стороны ЖКТ. Но Диклофенак и сегодня считается очень эффективным лекарством, его назначают короткими курсами для снятия боли и воспалительного процесса. Для мазей с НПВП ограничений в применении нет.

Симптоматические препараты для медикаментозного лечения
НПВП, подавляющие только ЦОГ-2 (Нимесулид, Мелоксикам), – это лекарства нового поколения. Они обладают селективным (избирательным) действием и почти не имеют побочного действия на ЖКТ при правильном применении. Они также применяются в современной практике.
Глюкокортикоидные гормоны
Глюкокортикоиды (Преднизолон, Дексаметазон, Метипред) назначаются при тяжелом течении ревматоидных процессов, сильных болях и поражении внутренних органов. В зависимости от состояния пациента эти препараты назначают или достаточно длительно малыми дозами (например, пожилым больным с противопоказаниями для базисной терапии), или короткими курсами очень большими дозами (пульс-терапия). Введение гормональных препаратов в полость сустава может приостановить его воспаление и формирование контрактуры.
Синтетические базисные противовоспалительные препараты
Синтетические базисные препараты применяются достаточно давно, но не потеряли своей актуальности. Курс начинается с назначения одного препарата этой группы. При высокой активности РА лечение начинают с Метатрексата, при средней и небольшой – с Сульфасалазина или Плаквенила. За эффективностью терапии тщательно наблюдают и если эффект есть, но недостаточный, присоединяют еще один базисный препарат (синтетический или биологический). Если эффекта нет, препарат меняют.
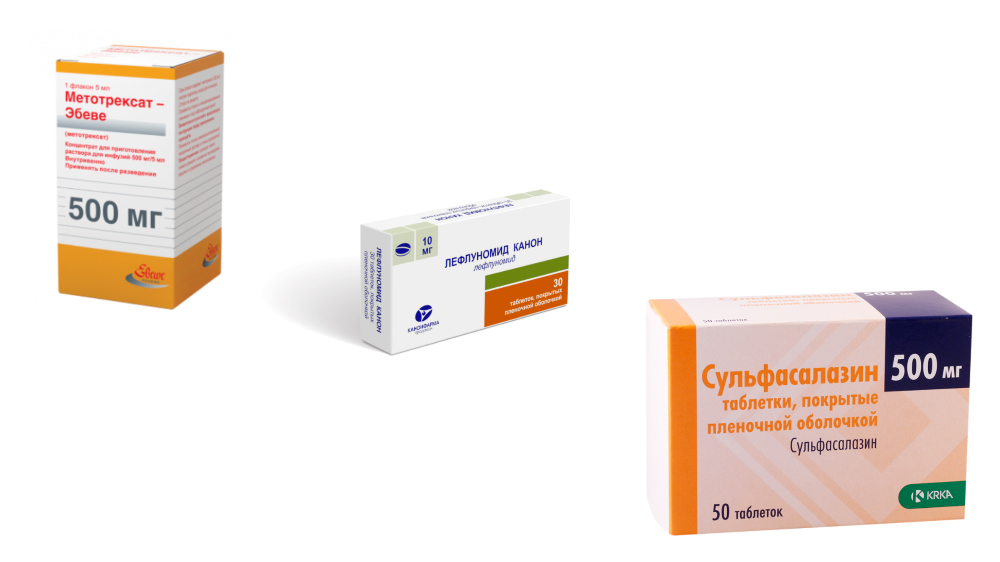
БПВП первого ряда для лечения ревматроидного артрита
Биологические (генно-инженерные) БПВП – биологические агенты
Это новый метод лечения ревматоидного артрита. Лекарства данной группы - препараты нового поколения, оказывающие прицельное действие на провоспалительные (поддерживающие ревматоидное воспаление) цитокины (ИЛ-1, ФНО- альфа) или на рецепторы иммунных клеток лимфоцитов. Избирательность действия этих препаратов нового поколения позволяет свести к минимуму их побочные эффекты:

Метипред – стероидный противовоспалительный препарат, который обладает широким спектром действия. Он эффективен при различных воспалительных процессах, вызванный вирусной инфекцией, в том числе при коронавирусе. Его назначают в комплексе с другими группами лекарственных средств, которые влияют на причины и симптомы заболевания. Схема приема Метипреда при коронавирусе назначается индивидуально, по результатам анализов – эти таблетки можно пить только после обследования у врача.
Состав и форма выпуска
Метипред – это гормональное (стероидное) противовоспалительное средство. В его составе содержится метилпреднизолон. Это вещество представляет собой гормон, синтезированный в лабораторных условиях – по строению он является аналогом гормона надпочечников человека. Он обладает выраженным противовоспалительным действием, благодаря чему нашел применение при острых состояниях, системных и аутоиммунных заболеваниях.
Метипред представлен в форме таблеток для приема внутрь. Они крупные, белого цвета. В них может содержаться 4 либо 16 мг метилпреднизолона. Таблетки находятся в упаковках по 30 либо 100 штук.
Важно:
Препараты на основе метилпреднизолона, в том числе Метипред, применяются для лечения серьезных воспалительных процессов. Их не принимают без острой необходимости, в связи с высоким риском побочных эффектов.
Механизм действия при коронавирусе
Метипред – эти таблетки для приема внутрь. Действующее вещество высвобождается и всасывается через слизистые оболочки пищеварительного тракта. У него высокая степень усвоения (до 70%) и быстрое действие – уже через 1,5 часа в крови наблюдается максимальная концентрация метилпреднизолона.
Активное вещество вызывает следующие эффекты в организме:
- противовоспалительный – влияет на воспалительные процессы на клеточном уровне;
- иммуносупрессии – подавляет работы иммунной системы, что необходимо при остром течении аутоиммунных заболеваний;
- противоаллергический – обусловлен снижением выработки и высвобождения гистамина и других медиаторов аллергии;
- общий стабилизирующий.
Метипред назначается при обструктивных и воспалительных заболеваниях дыхательных путей, в том числе при коронавирусе. Его эффективность обусловлена снижением активности воспалительных процессов и уменьшением проявления пневмонии. Кроме того, активные вещества препарата препятствуют отечности слизистых оболочек. В результате его приема уменьшается вероятность отложения слизи в альвеолах легких и в просвете бронхов, а также повреждения и некроза слизистых оболочек. При курсовом применении происходит купирование симптомов вирусной пневмонии.

Метипред доказал высокую эффективность при тяжелом течении вирусной пневмонии
Показания к применению препарата
Метипред – это гормональный противовоспалительный препарат широкого спектра действия. Его назначают при различный процессах, которые сопровождаются повышенной температурой, болью и ухудшением самочувствия. Врачи назначают это средство при следующих патологиях:
- системных заболеваниях, которые поражают соединительную ткань (системной красной волчанке, ревматоидном артрите и других);
- воспалительных болезнях суставов любого происхождения (остеоартрите, в том числе спровоцированном травмами, подагре, псориатическом и других видах артрита);
- бронхиальной астме;
- аллергических и аутоиммунных патологиях;
- болезнях крови и системы кроветворения;
- заболеваниях дыхательной системы, в том числе вирусной пневмонии.
Важно, что Метипред не является препаратом для лечения легкой степени коронавируса. Из-за большой вероятности побочных эффектов и большого количества противопоказаний его назначают при средней и тяжелой форме вирусной пневмонии. На начальных стадиях, при низком риске развития пневмонии, используют нестероидные противовоспалительные средства.
Схема приема при коронавирусе
Метипред представлен в форме таблеток для приема внутрь. Дозировку и режим приема назначает врач, в зависимости от возраста пациента, стадии болезни и наличия сопутствующих заболеваний. Средняя суточная доза составляет от 4 до 48 мг в сутки. Это количество принимают внутрь однократно, запивая водой. После снятия воспаления и достижения нужного эффекта дозировку можно уменьшать, но прием препарата продолжают до окончания курса лечения.
Детям суточную дозу Метипреда назначают индивидуально, в зависимости от веса. Средняя дозировка составляет от 0,42 до 1,67 мг на кг веса. Это количество необходимо разделить на 3 приема в день.
Справка:
Действующее вещество Метипреда проявляет внутриклеточную активность. Это значит, что препарат продолжает работать еще некоторое время после того, как перестает обнаруживаться в крови.

Метипред можно купить в обычной аптеке, но принимать его рекомендуется только после обследования врачом
Противопоказания и побочные эффекты
Препараты на основе преднизолона, в том числе Метипред, следует принимать только по назначению врача. Перед началом курса лечения важно убедиться в отсутствии противопоказаний. К ним относятся острые и хронические заболевания, а также патологические состояния, которые могут обостряться под действием гормональных противовоспалительных средств. Одно из противопоказаний к применению Метипреда – это грибковые заболевания. Также препарат не назначают во время беременности и грудного кормления.
С осторожностью средство используют в следующих случаях:
- острые и хронические заболевания желудочно-кишечного тракта (воспалительные процессы желудка и кишечника, язва желудка и двенадцатиперстной кишки);
- инфекционные заболевания вирусного, бактериального либо грибкового происхождения, в том числе опоясывающий лишай, герпес, корь и другие;
- период в несколько недель до и после вакцинации;
- патологии эндокринной системы и обмена веществ (тиреотоксикоз, гипотиреоз, сахарный диабет);
- острые и хронические болезни сердечно-сосудистой системы, особенно сердечная недостаточность и перенесенный инфаркт миокарда.
Во время курса лечения важно следить за самочувствием. Препарат может вызывать ряд побочных эффектов, особенно в случае превышения назначенной врачом дозировки. В таблице указаны основные нарушения, которые могут проявляться во время приема лекарства.
| Область развития побочных эффектов | Проявления |
| Желудочно-кишечный тракт, печень | Воспалительные заболевания желудка и кишечника, тошнота и рвота, повышение активности печеночных ферментов |
| Сердечно-сосудистая система | Аритмии, различные изменения на ЭКГ, а также увеличение участка некроза после инфаркта |
| Иммунная система | Аллергические реакции: зуд, покраснение кожи, сыпь, дерматиты, отечность слизистых оболочек |
| Опорно-двигательный аппарат | Слабость мышц и их атрофия, остеопороз, а также задержка роста и развития у детей |
| Общие нарушения | Ухудшение самочувствия, ухудшение заживания ран |
При появлении побочных эффектов необходимо отменить курс лечения либо корректировать дозу. В остальных случаях не рекомендуется резко прерывать прием препарата. Дозировку снижают постепенно, после чего можно полностью прекращать лечение.
Полезные советы
Совет № 1
Метипред – это сильнодействующий препарат, который используется при среднем и тяжелом течении коронавируса. Его следует принимать только под контролем лечащего врача и следить за самочувствием. Если пить его самостоятельно, есть риск развития осложнений и опасных побочных эффектов.
Совет № 2
Гормональные противовоспалительные препараты, в том числе Метипред, с осторожностью комбинируют с другими лекарственными средствами. Он может влиять на их эффективность, повышая либо снижая ее. Подобрать точную схему, которая не будет вредить здорово, сможет лечащий врач, с учетом результата анализов.
Совет № 3
Метипред при коронавирусе не используют самостоятельно. Схема лечения будет включать различные препараты, в том числе симптоматические. Они помогают уменьшить воспалительный процесс в дыхательных путях, восстановить слизистые оболочки и остановить кашель. Только полная схема, которая будет влиять на все этапы развития болезни и ее симптомы, приводит к быстрому результату.

Метипред эффективен как самостоятельно, так и в сочетании с лекарственными средствами других групп
Частые вопросы
Можно ли вылечиться Метипредом от коронавируса?
Метипред часто используется для лечения коронавируса, в том числе для больных со средним и тяжелым течением. Он доказал высокую эффективность, но используется только по назначению врача.
Можно ли приобрести Метипред в аптеке и принимать его самостоятельно при коронавирусе?
Препарат есть в наличии в аптеках, поэтому его можно купить и пить при коронавирусе. Однако, средство относится к сильнодействующим, поэтому перед его применением важно проконсультироваться с врачом.
Как правильно принимать Метипред для лечения коронавируса?
Таблетки принимают курсом, по одной или две в день. Дозировка может существенно отличаться при разных стадиях болезни, а также с учетом результатом анализов. Подобрать оптимальную схему поможет лечащий врач.
Мне 70 лет.принимаю метипред по 2е таблетки после ковида, можно продолжить пить сермион и канкор ? Спасибо
Добрый день. Ревматолог назначила метипред по 1т.утром. Терапевт сказала, чтобы не испортить желудок надо пить омепразол параллельно. Вопрос, надо ли принимать Омез постоянно с метипредом или курсами? Метипред пью уже полгода, диагноз Болезнь Шегрена.
Здравствуйте. Если врач не назначил иначе, то применяйте постоянно, пока применяете препарат метипред . По возможности очно проконсультируйтесь с врачом-гинекологом.
Доброго времени суток! Ревматоидный артрит, по назначению ревматолога принимаю метипред . По другому заболеванию терапевт назначил Артоксан 12 уколов по схеме. Подскажите, пожалуйста, можно ли колоть Артоксан, если утром принимаю метипред ? И если можно, то не будет это много - 12 уколов? Заранее благодарна за ответ.
Здравствуйте. При параллельном применении препаратов возможно увеличение риска развития желудочно-кишечных кровотечений.
Добрый день! Мама начала принимать препарат Форстео по рекомендации эндокринолога. Через неделю после начала приема попала в больницу с короновирусом. Лечащий врач велела отменить Форстео в связи с назначением гормональных препаратов. После выписки из больницы мама продолжает принимать гормоны ( Метипред ). Через какое время можно начинать Форстео? И не опасны ли такие перерывы в лечении препаратом Форстео?
Здравствуйте. Дальнейшее лечение препаратом Форстео возможно только после очной консультации с лечащим врачом (терапевтом, эндокринологом). Возможно потребуется коррекция терапии.
Здравствуйте. После выписки из больницы, где я лечила двухстороннюю полисегментарную пневмонию, мне назначили пить метипред по 3 таблетки утром 10 дней, затем снижать по 1/2 таб. каждые три дня до полной отмены. Можно ли принимать метипред одновременно с панангином, т.к. участился пульс до 100 ударов, или можно принимать другое лекарство от аритмии, давление в норме. Принимаю ещё эликвис. Спасибо заранее за ответ
Здравствуйте. Биологически активную добавку сидерал принимают по 1 капсуле 1 раз в день во время еды. Время суток значения не имеет.
Добрый вечер нет медрола 4 мг в городе совсем, можно ли взять 16 мг и разделить его в 4 раза или лучше взять его аналог метипред ?
Здравствуйте! У меня ревматоидный артрит с ноября 2020 года.Принимаю метипред и метотрексат. До болезни принимала конкор от давления и кардиомагнил.Сейчас все отменила и пью только проиворевматические препараты.Можно ли добавить кардимагнил и конкор сейчас?
Здравствуйте, пью метипред , по снижению, доза на сегодняшний день - 5 таблеток. Снижаю по четвертинке в неделю. Вопрос - сейчас обострился хронический герпес. Всегда лечилась в этих случаях амиксином. Возможно ли сейчас совместное применение метипред и амиксин? Спасибо!
Здравствуйте! У меня заложенность носа и вехних дыхательных путей с 23 мая. Прописали Метипред , а у меня остался прописанный раньше Лефлобакт. Не лучше ли его принимать, вместо Метипреда?
Здравствуйте. Нет, препарат Лефлобакт (левофлоксацин) не может служить заменой назначенному Вам препарату Метипред (метилпреднизолон).

Обзор
Моноклональные антитела — новая надежда в лечении ревматических заболеваний.
Автор
Редакторы


Теорию аутоиммунитета сформулировал еще столетие назад немецкий исследователь Пауль Эрлих. За последующие годы описано множество аутоиммунных заболеваний. К ним относятся ревматоидный артрит, системная красная волчанка (СКВ), системная склеродермия, миопатии, васкулиты и прочие патологии .
Болезни, ассоциированные с аутоиммунным компонентом, — серьезная проблема современного общества . Их распространенность в мировой популяции составляет примерно 5%. Заболевания быстро переходят в хроническую форму, из-за чего снижается качество жизни пациентов. Аутоиммунные патологии часто приводят к инвалидизации больных [1], [4].
Несмотря на многолетний поиск новых путей фармакотерапии, современная медицина не может предложить способов лечения, непосредственно влияющих на причину возникновения аутоиммунитета. Врачи способны лишь замедлить прогрессирование патологии и снизить выраженность клиники — провести патогенетическое и симптоматическое лечение. Для этого разработана базисная терапия, которая применяется уже многие годы. Однако не всегда проверенные препараты работают так, как надо.
Почему необходимо искать новые способы лечения?
Для лечения аутоиммунных заболеваний используют широкий арсенал противоревматических лекарств. Классическая терапия включает нестероидные противовоспалительные средства, глюкокортикоиды, цитостатики. В зависимости от особенностей развития заболевания подбирают препараты из той или иной группы [4].
Лекарства, применяемые при ревматических болезнях
- Большие иммунодепрессанты:
- глюкокортикоиды (преднизолон, дексаметазон);
- антибиотики (циклоспорин, такролимус);
- антиметаболиты (метотрексат, азатиоприн, меркаптопурин);
- цитостатики (циклофосфан).
- Малые иммунодепрессанты:
- плаквенил, хингамин;
- купренил;
- препараты золота (ауронофин);
- гепарин;
- нестероидные противовоспалительные средства.

Рисунок 2. Структурные формулы метотрексата и фолиевой кислоты. Препарат (а) по строению похож на фолиевую кислоту (б). Он состоит из птеридиновых групп и парааминобензойной кислоты. Действующий компонент метотрексата отличается от структуры фолата отсутствием гидроксильной группы (–OH) и наличием дополнительного метильного радикала (–CH3).
По механизму действия метотрексат относится к антиметаболитам. Препараты этой группы тормозят физиологические реакции в организме, связываясь с ферментами и выключая их активность. Вещество, которое в норме участвует в реакции, уже не может попасть в биохимический круговорот из-за повышенной конкуренции с компонентами лекарства. Основной мишенью для действия метотрексата является фермент, расщепляющий фолиевую кислоту, — дигидрофолатредуктаза (ДГФ). Этот белок воздействует на поступающий в организм фолат, переводя его в активную форму. При этом образуется тетрагидрофолиевая кислота. Она участвуют в синтезе строительного материала для ДНК — пуриновых оснований и тимидилата.
Метотрексат вклинивается в цепочку реакций благодаря структурному сходству с молекулой фолиевой кислоты (рис. 2). Конкуренция за фермент приводит к тому, что содержание активного фолата в ткани значительно снижается. Нет строительного материала — нет и новых молекул ДНК, без которых клетки не могут размножаться. Повышенной чувствительностью к воздействию лекарства обладают те ткани, структурные элементы которых постоянно делятся. К ним относятся и компоненты костного мозга, из которых формируются будущие иммунные клетки.
Еще один важный момент в работе метотрексата связан с активностью его полиглутамированных метаболитов. Эти молекулы формируются после активации препарата непосредственно в клетках человеческого организма. Они ингибируют другие ферменты, которые взаимодействуют с фолиевой кислотой. В эту группу входят тимидилсинтетаза и АИКАР-трансамилаза. Активность производных метотрексата запускает процесс выработки аденозина. Он оказывает мощное противовоспалительное действие, благодаря чему снижается выраженность симптомов ревматоидного артрита [7].
Метотрексат удобно использовать — он легко дозируется и может назначаться длительными курсами. Кроме того, важное преимущество этого препарата — низкая цена, в сравнении с современными лекарствами импортных фармкомпаний [8]. Несмотря на все достоинства, лечение метотрексатом не всегда приводит к снижению активности заболевания. У многих пациентов использование препарата неэффективно даже в комбинации с другими классическими средствами [5]. Это подтверждается при анализе статистики. Исследования показали, что при проведении лечения метотрексатом и комбинациями базисных препаратов только половина пациентов достигла ремиссии [9], [10].
Несостоятельность классической терапии заставляет ученых искать новые способы лечения ревматоидного артрита. Стоит отметить, что, несмотря на новые разработки, борьбу с заболеванием все же начинают с назначения метотрексата и его аналогов. Дополнительные препараты используют только при высокой активности аутоиммунного процесса. У таких пациентов применение одного лекарства часто бывает неэффективно [7]. В зависимости от особенностей течения патологии подбирают подходящую схему терапии (рис. 3).

Рисунок 3. Тактика ведения пациента с ревматоидным артритом при неэффективности использования метотрексата.
Неэффективность препаратов базисной терапии встречается не только при ревматоидном артрите, но и при других заболеваниях аутоиммунного происхождения (системной красной волчанке, склеродермии, болезни Бехтерева). Это мотивирует специалистов-ревматологов разрабатывать другие лекарства и подбирать новые схемы терапии.
Генно-инженерные препараты: дополнение к базисной терапии
По-новому взглянуть на лечение аутоиммунных заболеваний позволила разработка терапевтических моноклональных антител [11]. Принципиально новый класс препаратов получен благодаря достижениям генной инженерии. Для понимания механизма действия этих лекарств стоит вспомнить о том, как работают иммунные клетки в норме и при патологии [1], [12].
При аутоиммунных заболеваниях можно подавлять сразу весь сложный механизм иммунитета, что и делают препараты классической терапии. Но это оставляет человека без защиты от вражеских агентов — бактериальных инфекций, вирусов и прочих патогенов. Поэтому предпочтительнее сохранить активность иммунной системы в целом, избавив человека от аутоагрессии определенных ее компонентов. Именно так работают новые препараты — моноклональные антитела.
- Ингибиторы ФНО (фактора некроза опухолей) — инфликсимаб, этанерцепт, цертолизумаб, голимумаб, адалимумаб.
- Блокаторы интерлейкиновых рецепторов — тоцилизумаб (ИЛ-6R), канакинумаб (ИЛ-1R), секукинумаб (ИЛ-17R).
- Анти-В-клеточные антитела (антитела к мембранным молекулам CD20) — ритуксимаб, белимумаб [17].
- Анти-Т-клеточные антитела (антитела к молекулам CD80 и CD86) — абатацепт [18].
Ингибиторы ФНО
Ингибиторы фактора некроза опухолей — это первые моноклональные антитела, внедренные в ревматологическую практику. В эту группу входят инфликсимаб, этанерцепт, цертолизумаб, голимумаб, адалимумаб.
Фактор некроза опухолей (ФНО) — это провоспалительный цитокин (вещество, которое стимулирует развитие воспалительной реакции). В норме при его выделении происходит пролиферация клеток сосудов, активация макрофагов, лизис опухолевых агентов. Эти эффекты играют важную роль в защите организма от патогенов. Воспаление можно считать ответной реакцией на воздействие повреждающих факторов.

Рисунок 5. Патологические изменения в суставе при ревматоидном артрите. Аутоиммунный процесс вызывает появление эрозий, синовит (воспаление синовиальной оболочки), разрушение суставного хряща.
Такое строение связано с механизмом получения препарата. Первоначально синтезируют антитело к фактору некроза опухолей в организме мыши. Полученный иммуноглобулин специфичен к ФНО и уже может его обезвреживать, но полностью чужеродные белки вводить в организм пациентов, конечно, нельзя. Это вызовет активную иммунную реакцию — выработку антител уже против терапевтических агентов. Поэтому домены мышиного иммуноглобулина заменяют сходными участками человеческих белков. Антитела, имеющие фрагменты разного происхождения, называются химерными. Фактически, они берут лучшие качества своих предшественников. Мышиная часть обеспечивает высокую чувствительность к ФНО, а человеческие фрагменты снижают иммуногенность — вероятность развития иммунного ответа.

Рисунок 6. Основные эффекты ФНО и блокирующие его моноклональные антитела (инфликсимаб и этанерцепт). Мишенями для моноклональных антител являются свободная и мембраноассоциированная формы фактора некроза опухолей. Лекарства препятствуют связыванию цитокина с рецептором, благодаря чему снижается активность ревматоидного артрита.
Блокаторы интерлейкиновых рецепторов
В развитии аутоиммунного воспаления важную роль играют интерлейкины, которые, как и ФНО, относятся к провоспалительным цитокинам (рис. 7). Основными представителями этой группы являются ИЛ-6, ИЛ-1, ИЛ-17. Функция интерлейкинов — это контроль процессов дифференцировки, пролиферации и гибели (апоптоза) иммунных клеток, который осуществляется через соответствующие гены-мишени [20].

Рисунок 7. Механизм действия интерлейкинов при аутоиммунном воспалении (на примере ИЛ-6). Цитокин влияет на T- и B-лимфоциты, гемопоэтические клетки, гепатоциты. Он стимулирует выработку аутоантител В-клетками, а также формирование аутореактивных Т-клонов, которые непосредственно участвуют в аутоиммунном процессе. Влияние на костный мозг заключается в стимуляции выработки новых клеток крови — повышается число лейкоцитов и тромбоцитов. Воспаление сопровождается ответной реакцией клеток печени, появлением характерных симптомов аутоиммунного заболевания.
Тоцилизумаб — это препарат, который блокирует работу ИЛ-6. Рецептор этого вещества состоит из двух компонентов — мембранного ИЛ-6R (α-цепь) и гликопротеина g130 (β-цепь). Мембранная часть рецептора связывается с ИЛ-6, образуя устойчивый комплекс. Вместе они активируют компонент g130, вызывая изменение его структуры (гомодимеризацию). Образуется рецепторный комплекс из двух молекул g130, который в свою очередь активирует JAK1-киназу. Этот фермент запускает каскад реакций в клетке, который приводит к появлению биологического эффекта цитокина — развитию воспаления. В некоторых случаях ИЛ-6 связывает не мембранная, а растворимая форма α-цепи (рис. 8). Механизм действия рецептора при этом не меняется [21].
В основе работы тоцилизумаба лежит конкуретное ингибирование. Сигнальные молекулы активно связываются с моноклональным антителом. Вакантное место занято — интерлейкин не может образовать комплекс с рецептором, а значит, он не способен активировать процесс воспаления.

Рисунок 8. Механизм действия тоцилизумаба. Препарат связывает растворимые и мембранные рецепторы ИЛ-6, блокируя передачу сигналов.
Тоцилизумаб считается одним из самых безопасных препаратов, входящих в группу моноклональных антител. Это позволяет применять его при ювенильном идиопатическом артрите, который возникает в возрасте до 16 лет. Дети особенно остро реагируют на токсические воздействия, поэтому препараты, которые используют при их лечении, должны иметь минимальное число побочных реакций. Применение тоцилизумаба позволяет достигнуть необходимого эффекта лечения, не вызвав тяжелых осложнений.
Анти-B-клеточная терапия
Препараты из группы анти-B-клеточной терапии (ритуксимаб и белимумаб) блокируют активность В-лимфоцитов путем связывания их мембранных молекул CD20. Эти вещества есть только у определенных категорий В-клеток. Они специфичны для пре-В-лимфоцитов и зрелых В-лимфоцитов. CD20 нет у стволовых элементов и про-В-клеток, из которых будут образовываться новые лимфоцитарные элементы. Мембранные молекулы данного типа не содержатся и у плазматических клеток, которые вырабатывают иммуноглобулины [22].

Рисунок 9. Механизм работы ритуксимаба. Fab-фрагмент моноклонального антитела связывается с CD20 на поверхности B-лимфоцита. Это запускает лизис клетки, который может осуществляться несколькими путями: через систему комплемента, программу апоптоза или агрессию натуральных киллеров и макрофагов.
Анти-Т-клеточная терапия
Блокировка действия Т-лимфоцитов возможна благодаря особенностям их активации. Чтобы Т-лимфоцит вступил в аутоиммунный процесс и связался с антигеном, он должен получить два сигнала от антигенпрезентирующих клеток (АПК). Первый сигнал обеспечивает распознавание специфического аутоантигена Т-клеточными рецепторами. Второй сигнал — это неспецифический процесс связывания мембранных молекул CD80 и CD86 на поверхности АПК с рецептором CD28 лимфоцита. Сочетание этих взаимодействий вызывает активацию Т-клеток, которые в свою очередь стимулируют выработку провоспалительных цитокинов. Это и есть основной вклад Т-лимфоцитов в аутоиммунный процесс.
Знания о механизме активации Т-клеток использовали при разработке моноклональных антител. Основной представитель анти-Т-клеточных агентов — это абатацепт. Препарат представляет собой белок, состоящий из двух частей. Специфическая часть образована молекулой CTLA-4 (антиген 4 цитотоксических лимфоцитов). Неспецифическая область — это Fc-фрагмент человеческого иммуноглобулина G1 [23].
Воздействие абатацепта направлено как раз на неспецифический (костимулирующий) сигнал. Компонент CTLA-4 связывает белки CD80 и CD86 на поверхности антигенпрезентирующих клеток. Рецептор лимфоцита CD28 уже не может взаимодействовать с ними, из-за чего активация Т-клетки не завершается (рис. 10).

Рисунок 10. Механизм действия абатацепта. Абатацепт модулирует иммунный ответ через связывание с CD80/CD86 на антигенпрезентирующих клетках. Это препятствует связыванию CD80/CD86 с CD28 T-клеток, то есть активация Т-клеток отменяется через блокировку костимуляции.
Не всё так просто: возможные проблемы при использовании моноклональных антител
Например, одна пачка метотрексата стоит примерно 200 рублей. Цена упаковки инфликсимаба — около 43 тыс. рублей. Разница очевидна. За год лечения метотрексатом даже в максимальной дозировке пациент потратит на лекарство 1–2 тыс. рублей (в зависимости от фирмы-производителя, схемы лечения и стоимости препарата в местных аптеках). Цена годовой терапии инфликсимабом составляет примерно 700 тыс. рублей. Понятно, что самостоятельно обеспечить себя этим лекарством сможет только очень ограниченная группа пациентов.
Использование биологических препаратов допустимо в тех случаях, когда к базисным средствам у пациента развивается непереносимость. Больные испытывают тяжелое побочное воздействие лекарства, которое еще сильнее ухудшает их состояние. Применение препаратов с другим механизмом действия, в том числе и моноклональных антител, позволяет минимизировать побочные эффекты [18].
Другая сложность, с которой можно столкнуться при использовании биологических препаратов, — это побочные реакции. Параллельно с накоплением данных об эффективности использования лекарств выявляют все новые нежелательные эффекты от их применения. Большая часть таких реакций связана с процессом иммуносупрессии. Подавляя активность иммунных клеток, моноклональные антитела снижают защитную функцию организма. В первую очередь страдают противоинфекционный и противоопухолевый иммунитеты [18], [24].
Парадоксально, но применение новых лекарств против аутоиммунитета может вызвать острые аутоиммунные реакции. Все биологические препараты представляют собой белковые молекулы, которые в той или иной степени чужеродны для организма. Поэтому при проникновении терапевтических агентов в тело больного иммунитет может распознать их как антигены. Появляется активный иммунный ответ — вырабатываются антитела уже против компонентов препарата.
Несмотря на все возможные сложности, моноклональные антитела прочно вошли в регистр лекарств, применяющихся в ревматологии. Перспектива использования биологических препаратов и их место в ревматологии будет зависеть от результатов многолетних исследований, которые еще предстоит провести. Но даже сейчас можно сказать, что разработка терапевтических моноклональных антител является важным шагом на пути к победе над аутоиммунным воспалением.
Читайте также:

